Aktue Hirnverletzungen
Gliazellen spielen bedeutende Rolle für die Umbildung der Blutgefäße
Gliazellen und insbesondere Astrozyten ermöglichen einen Austausch zwischen Nervenzellen und Blutgefäßen im Gehirn. Bei den häufigsten Hirnschädigungen, wie z. B. Schädel-Hirn-Trauma und Schlaganfall, wird dieser Austausch jedoch stark beeinträchtigt und führt zu einer Verschlechterung des Stoffwechsels, wodurch sich die anfängliche Erkrankung verschlimmert. Astrozyten haben sich als wichtige Zellen für die Reparatur des Hirngewebes herausgestellt, wobei die zugrundeliegenden Mechanismen bislang nur unzureichend verstanden werden. Forschende des Max-Planck-Instituts für Biologie des Alterns und des Exzellenzclusters CECAD in Köln konnten jetzt zeigen, dass eine akute Hirnverletzung und die Störung der Blut-Hirn-Schranke die Bildung ausgeprägter, mit Mitochondrien angereicherter Zellstrukturen, in den Astrozyten hervorrufen. Diese ermöglichen eine Umbildung der Blutgefäße. Die Studie erschien in der Fachzeitschrift „Cell Metabolism“.
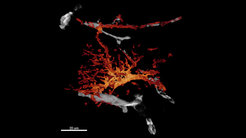
Schädel-Hirn-Traumata und Schlaganfälle gehören weltweit zu den häufigsten Todesursachen. Patienten erleiden oft erhebliche Beschädigungen der Blutgefäße des Gehirns, welche unweigerlich von Hirnblutungen, sekundärer Entzündung und neuronalem Funktionsverlust begleitet werden. Matteo Bergami, einer der zwei Studienleiter, sagt hierzu: „Mehrere Faktoren tragen zum Ausmaß des primären Gewebeschadens bei. Wir fangen jedoch erst an, die Mechanismen der Gefäßneubildung und der Genesung des Hirngewebes in der geschädigten Hirnregion vollständig zu verstehen.“
Um einen tieferen Einblick in diese Mechanismen zu erlangen, fokussierten sich die Wissenschaftlerinnen und Wissenschaftler auf einen bestimmten Typ von Gliazellen, die Astrozyten, deren spezialisierte Prozesse in der Nähe der Blutgefäße die Versorgung des Nervenzellgewebes mit Stoffwechselprodukten gewährleisten. Ihre Versuche zeigen, dass Hirnverletzungen und die dadurch ausgelöste Schädigung der Blutgefäße die Umgestaltung von Mitochondrien und des endoplasmatischen Retikulums (ER) veranlassen, zweier zellulärer Organellen, die für diese perivaskulären Prozesse unentbehrlich sind. Die Umgestaltung der Organellen führt zur Ausbildung einer räumlich begrenzten, metabolisch aktiven Struktur, die die neu gebildeten Blutgefäße umgibt. „Wir haben eine solche Umstrukturierung der Organellen um Blutgefäße herum nicht erwartet, vor allem nicht in einem voll entwickelten, erwachsenen Gehirn. Das erscheint mir nur dann sinnvoll, wenn Astrozyten aktiv am Umbau der Blutgefäße beteiligt sind“, erklärt Jana Göbel, die frisch promovierte Erstautorin der Studie.
Die Forschenden nutzten anschließend neuartige Herangehensweisen, um die dynamischen Prozesse der beiden Organellen in Astrozyten gezielt zu verändern. Zudem beeinflussten sie die physischen Interaktionen der beiden Organellen miteinander, welche bereits in vorherigen Studien als grundlegender Faktor für bestimmte Stoffwechselfunktionen der Zelle beschrieben wurden. Wird die Zunahme an Kontaktpunkten zwischen Mitochondrien und ER verhindert, wirkt sich das erheblich auf die Komplexität des neu geformten Blutgefäßsystems aus, während andersherum die Förderung dieser Kontakte nach einer Hirnverletzung die Erneuerung eines fein verzweigten Gefäßsystems bewirkt. „Diese Ergebnisse sind wirklich faszinierend“, führt Elisa Motori aus, die zweite Studienleiterin, die für die Studie neue Mikroskopier- und Stoffwechselanalysemethoden ausgearbeitet hat. „Sie enthüllen eine komplett neue Ebene der Komplexität, auf welche Weise physische Interaktionen zwischen Mitochondrien und anderen Organellen eine Basis für die Formbarkeit von Hirnzellen und die Neuanordnung von Gewebe schaffen, die wir hoffentlich in zukünftigen klinischen Studien ausnutzen können.“
Die gemeinschaftliche Studie von Forschenden des CECAD und des Max-Planck-Instituts für Biologie des war nur durch die sich ergänzende Expertise innerhalb des Sonderforschungsbereichs (SFB) 1218 möglich. In konzeptioneller wie auch in technologischer Hinsicht stellt die Studie einen Fortschritt für das Verständnis dar, wie Gehirnzellen die Funktion und die dynamischen Prozesse von Organellen im erkrankten Organismus einbeziehen. Sie hat eine wesentliche Bedeutung für zahlreiche neurologische und zerebrovaskuläre Erkrankungen und bietet die Möglichkeit für gezielte Eingriffe, um die Genesung des Gehirns, beispielsweise nach einem Trauma, zu beschleunigen.












