Forschung
Affiliated-Forschungsgruppe Pernas
Intrazelluläre Krankheitserreger sind von den Metaboliten des Wirtes abhängig und konkurrieren daher mit den Stoffwechselprozessen um eine begrenzte Anzahl von Nährstoffen. Hauptakteure in diesem Wettbewerb sind die Wirtsorganellen, die bestimmte Metabolite speichern, abbauen, nutzen, importieren und exportieren.
Kürzlich konnten wir ein Beispiel für den Wettbewerb zwischen Organellen und Mikroben definieren: Während einer Infektion nutzt der menschliche Parasit Toxoplasma gondii den Abbau von Fetttröpfchen des Wirtes, um Zugang zu den für sein Wachstum essentiellen zellulären Fettsäuren zu erhalten. Um dies zu verhindern, fusionieren die Wirtsmitochondrien während der Infektion, um die Aufnahme von Fettsäuren zu verbessern. Damit limitieren sie den Zugang zu einer wichtigen Wirtsressource und schränken das Wachstum des Parasiten ein.
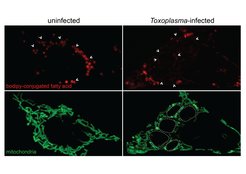
Diese Arbeit zeigt, dass Mitochondrien, die im Wesentlichen domestizierte Parasiten sind, aktiv und metabolisch die Zelle während der Infektion verteidigen. Allerdings bleiben weitere wichtige Aspekte über die Rolle der Wirtsorganellen und des Stoffwechsels bei der Ausführung der zellulären Reaktion auf die Infektion ungeklärt. Mit Toxoplasma gondii als Modellpathogen wollen wir daher folgenden Fragen nachgehen:
Wie erkennen und reagieren Zellorganellen auf intrazelluläre Krankheitserreger?
Nachdem wir bereits eine mitochondriale Reaktion auf Toxoplasmen definieren konnten, bleiben nun viele Fragen über die Signale, die es den Mitochondrien ermöglichen, Toxoplasmen zu erkennen und metabolisch auf sie zu reagieren. Darüber hinaus vermuten wir, dass sich der Wettbewerb zwischen Organelle und Mikrobe auf viele andere Organellen wie Lipidtröpfchen, Peroxisomen und das endoplasmatische Retikulum erstreckt, die während der Infektion zu mehreren intrazellulären Krankheitserregern gelangen und diese umgeben. Wir wollen verstehen, wie diese Reaktionen der Zellorganellen organisiert sind und welche Rolle sie im zellulären Infektionsprozess spielen.
Leiten Zellen ihre Stoffwechselwege um, damit Krankheitserregern der Zugang zu den für ihr Wachstum wichtigen Nährstoffen verwehrt bleibt?
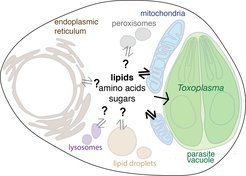
Wenn der Zugang zu Nährstoffen für einen Erreger durch Stoffwechselprozesse des Wirtes eingeschränkt werden kann, wäre eine logische Vorhersage, dass der Wirtsstoffwechsel als Teil der zellulären Reaktion auf eine Infektion aktiv neu verdrahtet wird. Zum Beispiel, um den Abfluss zu erhöhen oder den Import von Nährstoffen zu begrenzen, die für das mikrobielle Wachstum wichtig sind. Wir arbeiten daran diejenigen Wirtsstoffwechselwege zu definieren, die das Ergebnis der Infektion beeinflussen, und analysieren, wie die Neuverkabelung dieser Wege das Wachstum des Parasiten moduliert. Des Weiteren wollen wir verstehen, wie sich in verschiedenen Geweben die zellulären Reaktionen auf eine Infektion unterscheiden. Warum, zum Beispiel, können Toxoplasmen im Skelettmuskel ein Leben lang bestehen?
Was ist das Geheimnis des metabolischen Erfolgs von Toxoplasma?
Toxoplasma ist für mehrere Metabolite auxotroph, schafft es aber sich in wild variierenden Stoffwechselumgebungen (praktisch in jeder Zelle mit Zellkern in verschiedensten Säugetierwirten) zu vermehren. Unser Ziel ist es das Repertoir des Pathogens zu definieren, mit dem es den Wirt wahrnimmt und sich dessen Stoffwechsel anpasst (z.B. Effektorproteine, die das Abfangen von Wirtsmetaboliten ermöglichen / Wirtsstoffwechselprozesse modulieren). Das Erfassen dieses Repertoires bietet uns das Potenzial, die stoffwechselbedingte Achillesferse des Parasiten zu enthüllen, die für therapeutische Angriffe geeignet ist.
Die Antworten auf diese Fragen sind der Schlüssel zu einem tieferen Verständnis der Wirt-Pathogen-Interaktion und der Wirts-Stoffwechselnetze, die die Anfälligkeit für Infektionen bestimmen. Schließlich erhoffen wir uns, dass die Ergebnisse aus der Arbeit für menschliche Krankheitserreger übersetzt werden und wir somit zu dem Verständnis gelangen können, wie der menschliche Stoffwechsel das Fortschreiten von Infektionskrankheiten beeinflusst.

